بوابة:الكيمياء
|
مرحبًا بِكُم في بَوَّابَةِ ٱلْكِيمْيَاء |
| بوابة | مشروع | تصنيفات |
مُقدِّمة  عِلْم الكِيِمْيَاء هو العلم الذي يدرس المادة والتغيرات التي تطرأ عليها، وتحديدًا تتم دراسة خواصها، وبنيتها، وتركيبها، وسلوكها، وتفاعلاتها، والتداخلات التي تحدثها. ويَدرُسُ علم الكيمياء الذرات والروابط التي تحدث بينها مكونةً الجزيئات، وكيف تترابط هذه الجزيئات فيما بعد لتكوِّن المادة. وتدرس أيضًا التفاعلات التي تحدث بينها. وللكيمياء أهمية كبيرة في حياتنا وتدخل في مجالات كثيرة وتلعب دورًا مهمًا في الصناعات بمختلف أنواعها، كالصِّناعات الغذائية وصناعة المواد التنظيفية والدهانات والأصبغة وصناعة الأدوية والعقاقير والنسيج والملابس والأسلحة... وغيرها. ولها تطبيقات أخرى في الطب والعلوم الأخرى. ويطلق على الكيمياء تسمية «العِلْمُ المَرْكَزِي»، وذلك لدوره الجوهري في ربط العلوم الطبيعية ببعضها، وعلم الكيمياء هو أحد العلوم الطبيعية، والتي تشمل كلًا من الفيزياء وعلوم الأرض وعلم الفلك وعلم الأحياء. ويُعد تاريخ صناعة الكيمياء ذا أثرٍ بالغ في مجال الكيمياء بشكل عام. تدرس الفيزياء المادة أيضًا، ولكنها تدرس كميات الفضاء، والمادة، والقوانين التي تحكمها، والكيمياء فرع من العلوم الفيزيائية ولكنها لا تتفرع عن الفيزياء. يعد جابر بن حيان الملقب بـ «أبو الكيمياء»، المؤسس الحقيقي لمفهوم علم الكيمياء، المبني على مفهوم التجريبية، إذ يقول: «إن واجب المشتغل في الكيمياء هو العمل وإجراء التجربة، وإن المعرفة لا تحصل إلاَّ بها» حتى أن العرب سمَّوا الكيمياء عامةً بـ «صَنْعَة جَابِر». كلمة كيماء ذات أصلٍ عربي، وتشتق الكلمة من المصدر كمي بمعنى أستر وأخفى، ووجهة ذلك تعتمد على الكتمان وتحريم إذاعتها وإفضاء أسرارها لغير أهلها لكون هدفها تحويل المعادن البخسة إلى ذهب وفضة. تنقسم الكيمياء إلى فروع عدة تتفرع منها أقسام أخرى، أهمها: الكيمياء العامة والتي تدرس المبادئ الأساسية في الكيمياء، والكيمياء العضوية وتهتم بدراسة المواد العضوية، أي التي تحتوي على عنصر الكربون، والكيمياء الغير عضوية والكيمياء الفيزيائية والكيمياء الحيوية والكيمياء التحليلية.
|
مقالة مختارة المُركب الكيميائي هو مادة كيميائية تكونت من عنصرين أو أكثر، بنسبة ثابتة تحدد تركيبه، فمثلا الماء (H2O) مركب يتكون من الهيدروجين والأكسجين بنسبة 1:2، وبصفة عامة فإن هذه النسبة يجب أن تكون ثابتة لبعض الاعتبارات الفيزيائية، وليس طبقا للاختيارات البشرية، ولهذا السبب فإن المواد مثل النحاس الأصفر تعتبر سبيكة وليست مركب. ومن الخواص المميزة للمركب أن له بنية كيميائية مميزة يعبر عنها عن طريق صيغة جزيئية، تصف هذه الصيغ نسبة الذرات الموجودة به، وعدد الذرات الموجودة في جزيء واحد من المادة، وعلى هذا فيكون شكل الإيثان C2H4 وليس CH2)، ويمكن عن طريق معرفة تلك الصيغ حساب الكتلة المولية للمركب، توجد عدة معرفات لتمييز المركبات الكيميائية منها رقم CAS (رقم لتعريف كل المركبات). ويمكن للمركبات أن يكون لها حالات عديدة. معظم المركبات توجد في هيئة صلبة. كما أن المركبات الجزيئية يمكن أن توجد أيضا في حالة سائلة أو غازية.
|
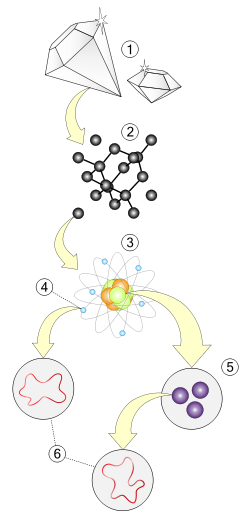
شخصية مختارة إرنست رذرفورد (30 أغسطس 1871 - 19 أكتوبر 1937) هو عالم فيزياء بريطاني مولود في نيوزيلندا والذي يعرف بـ"أب الفيزياء النووية" . تصنفه الموسوعة البريطانية كأفضل المجربين منذ مايكل فاراداي. اكتشف في أحد أعماله المبكرة العمر المنصف للعناصر المشعة، وأثبت أن النشاط الإشعاعي يشتمل على تحول العنصر الكيميائي إلى عنصر آخر، وفرق أيضاً وسمى أنواع الإشعاع إلى ألفا و بيتا. كل هذه الأعمال تمت في جامعة ماك جيل بكندا. مؤدية لحصوله على جائزة نوبل للكيمياء عام 1908، كما اكتشف نواة الذرة واقترح،سنة1911، نموذجا يشبه النظام الشمسي،حيث تشغل النواة المركز أما الإلكترونات فتدور حولها في مدارات دائرية. نال بعد ذلك منحة دراسية من جامعة كامبريدج في إنجلترا، ثم انتقل للعمل في معمل كافيندش العريق تحت إشراف العالم الكبير جوزيف جون طومسون مكتشف الإلكترون، وهناك اهتم بدراسة الأشعة الصادرة من عنصر الراديوم.
|
صور مُختارة |
عنصر مختار البروم عنصرٌ كيميائي رمزه Br وعدده الذرّي 35، ويقع في الجدول الدوري للعناصر ضمن عناصر الدورة الرابعة وفي المرتبة الثالثة ضمن مجموعة الهالوجينات؛ وتأتي خواصّه وسطاً بين جاريه الكلور واليود. عُزلَ هذا العنصر بشكلٍ مستقلٍّ من قبل كيميائِيَّين اثنين، وهما كارل ياكوب لوفيغ (في سنة 1825) وأنطوان جيروم بالارد (في سنة 1826)؛ واشتُقَّت تسمية هذا العنصر من الكلمة الإغريقية βρῶμος (بروموس)، وذلك بمعنى «نتن»، إشارةً لرائحته الكريهة. يوجد البروم في الظروف القياسية من الضغط ودرجة الحرارة على هيئة سائل مدخّن ذي لون بنّي محمرّ، وهو يعطي أدخنةً من نفس اللون. البروم والزئبق هما العنصران الوحيدان في الطبيعة اللذان يوجدان في الطور السائل عند درجة حرارة الغرفة. إنّ عنصر البروم نشيطٌ كيميائياً، ولذلك لا يوجد على شكله العنصري الحرّ في الطبيعة، ولكن على شكل مركّبات البروميدات؛ وتُسهّل الانحلالية المرتفعة لأيون البروميد من تجمّعه في مياه المحيطات؛ ومن السهل لذلك استحصال هذا العنصر تجارياً من البحيرات تحت سطح البحر. يشكّل البروم عدداً معتبراً من مركّبات البروم العضوية، والتي تتفكّك عند درجات حرارة مرتفعة لتعطي ذرّات البروم الحرّة، وهي عملية توقف تشكّل الجذور الكيميائية الحرّة في التفاعلات التسلسلية الكيميائية. تجعل هذه الظاهرة من مركّبات البروم العضوية مفيدةً في تثبيط الحرائق، وحوالي أكثر من النصف من كمّيّة البروم المنتجة عالمياً تُستخدَم لذلك الغرض. يحدث هذا التفكّك أيضاً عند تعرّض مركّبات البروم العضوية إلى الأشعّة فوق البنفسجية، ممّا يطلق ذرّات البروم الحرّة إلى الغلاف الجوّي مسبّباً نضوب الأوزون. لذلك فإنّ العديد من مركّبات البروم العضوية، مثل مبيد الآفات برومو الميثان، لم تعد في طور الاستخدام. من جهةٍ أخرى، لا تزال مركّبات البروم مستخدمةً في مجال سوائل الحفر وفي مجال أفلام التصوير الضوئي وفي صناعة الكيماويات العضوية.
|
هل تعلم؟ منشئ علم الكيمياء الحديثة هو العالم جابر بن حيان الأزدي ومن أهم انجازاته :
'
|
الكيمياء والمجتمع الكيمياء و المجتمع :  مطر حمضي - تلوث جوي - أمفيتامين - أسبيتوس - أسبارتام - أسبرين - كلوروفلوروكربون - كولسترول - كوكائين - كربوهيدرات - ثاني أكسيد الكربون - أسلحة كيميائية - إكستاسي - إنزيمات - استروجين - دهن - حمض دهني - جذور حرة - غازولين - كيمياء خضراء - وسائل منع النسل الهرمونيةهيروين - أنسولين - ثنائي إيثيل أميد حمض الليسرجيك - مورفين - وقود نووي - اندماج نووي - نايلون - أوزون - باراسيتامول - بنسلين - لدائن - عقار نفساني التأثير - نفايات مشعة - ضبخان - تلوث التربة - سكر - تاميفلو - تستوستيرون - فياغرا - فيتامين
|
أدوات مخبرية  شفاط — كأس زجاجي — أنبوب غليان — قمع بوشنر — موقد بنزن — سحاحة — مسعر — مقياس حرارة — مقياس لوني — مكيال مخروطي — رنين مغناطيسي نووي — مطيافية الكتلة — استشراب السوائل — استشراب الغازات — بوتقة — كويب مخبري — دوارق مخبرية (دورق تفريغ، دورق مخروطي، دورق الغليان، معوجة، دورق كروي، دورق حجمي) — كمة الدخان — محقنة غاز — أسطوانة مدرجة — مثلث بركن — ممص — كاشف كيميائي — قمع فصل — مقياس الطيف الضوئي — دورق شلينك — مؤشر الأس الهيدروجيني — ورقة عباد الشمس — ملقط — جهاز سوكسلت للاستخلاص — قضيب تحريك — خلاط سكوني — أنبوب اختبار — أنبوب ثيستل — مقياس اللزوجة |
تصنيفات |
محتوى مميز
|
الجدول الدوري
كتلة ذرية قياسية Ar, std(E)[1]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
أقسام الكيمياء الأساسية للكيمياء أقسام أساسية تتفرع منها الفروع الأخرى للكيمياء وهي: الكيمياء اللاعضوية تشمل: دراسة كل العناصر الموجودة في الجدول الدوري والمجموعات التي تنتمي إليها. الكيمياء العضوية تمثل: مركبات الكربون عنصر المجموعة الرابعة عشرة من الجدول الدوري كعنصر أساسي بالإضافة إلى عناصر أخرى. الكيمياء الفيزيائية: يعود نشوء الكيمياء الفيزيائية إلى منتصف القرن الثامن عشر. فقد أدت المعلومات التي تجمعت حتى تلك الفترة في فرعي الفيزياء والكيمياء إلى فصل الكيمياء الفيزيائية كمادة علمية مستقلة، كما ساعدت على تطورها فيما بعد. ولقد وضع العالم الروسي ميخائيل لومونوسوف أول كتاب جامعي في الكيمياء الفيزيائية. وهى دراسة الأصل الفيزيائي للتفاعلات والأنظمة الكيميائية. أو بمعنى آخر هو تداخل علم الكيمياء مع علم الفيزياء والطبيعة وكذلك فإنها تدرس تغييرات حالات الطاقة في التفاعلات الكيميائية. الكيمياء التحليلية: هي دراسة التركيب الكيميائي للمواد الطبيعية والاصطناعية. بخلاف الفروع الأخرى من الكيمياء مثل الكيمياء اللاعضوية أو الكيمياء العضوية فإن الكيمياء التحليلية غير محصورة بنوع محدد من المركبات أو بنوع معين من التفاعلات الكيميائية. الكيمياء الحيوية: هي أحد فروع العلوم الطبيعية ويختص بدراسة التركيب الكيميائي لأجزاء الخلية في مختلف الكائنات الحية سواء كانت كائنات دقيقة مثل (بكتيريا، فطريات، طحالب) أو راقية كالإنسان والحيوان والنبات. |
بوابات تتعلق بالكيمياء |
مشاريع شقيقة المزيد عن الكيمياء في المشاريع الشقيقة:
|
في القوالب |
- ^ Meija، Juris؛ وآخرون (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". Pure and Applied Chemistry. ج. 88 ع. 3: 265–291. DOI:10.1515/pac-2015-0305.
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. (4 May 2022). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry (بالإنجليزية). DOI:10.1515/pac-2019-0603. ISSN:1365-3075.